「化学/酸とアルカリ/酸の実体」の版間の差分
ナビゲーションに移動
検索に移動
編集の要約なし |
編集の要約なし |
||
| (同じ利用者による、間の11版が非表示) | |||
| 1行目: | 1行目: | ||
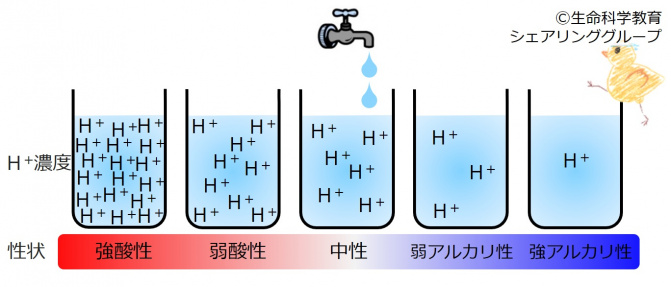
{{Point|水溶液中の水素イオン(H<sup>+</sup>)が多いほど酸性が強い。逆に、水素イオン(H<sup>+</sup>)が少ないほどアルカリ性が強い。}} | {{Point|水溶液中の水素イオン(H<sup>+</sup>)が多いほど酸性が強い。逆に、水素イオン(H<sup>+</sup>)が少ないほどアルカリ性が強い。}} | ||
[[ファイル: | [[ファイル:04390.jpg|none|671px]] | ||
酸の実体とは、水素イオン(H<sup> +</sup>)なのです。水溶液中の水素イオン濃度がその溶液の酸性、アルカリ性を決定します。 | 酸の実体とは、水素イオン(H<sup> +</sup>)なのです。水溶液中の水素イオン濃度がその溶液の酸性、アルカリ性を決定します。 | ||
真水にはH<sub>2</sub>Oしかないわけではないのです。ある一定濃度の水素イオン(H<sup> +</sup>)があります。 | 真水にはH<sub>2</sub>Oしかないわけではないのです。ある一定濃度の水素イオン(H<sup> +</sup>)があります。 | ||
<br><strong>水素イオン濃度が真水より 低い水溶液は <span style="background: lightsteelblue">アルカリ性</span>であり、高い水溶液は<span style="background: salmon">酸性</span> | |||
<strong>水素イオン濃度が真水より 低い水溶液は <span style="background: lightsteelblue">アルカリ性</span>であり、高い水溶液は<span style="background: salmon">酸性</span> | |||
</strong>です。また、 | </strong>です。また、 | ||
<strong> 水素イオン濃度が 低いほど<span style="background: blue">アルカリ性が強く</span>、 高いほど <span style="background: red">酸性が強い</span></strong> | <strong> 水素イオン濃度が 低いほど<span style="background: blue">アルカリ性が強く</span>、 高いほど <span style="background: red">酸性が強い</span></strong> | ||
のです。 | のです。 | ||
<br style="clear:both;" /> | |||
{{QuizTitle}} | {{QuizTitle}} | ||
<GIFT> | <GIFT> | ||
:: | //LEVEL:1 | ||
//RAND | |||
[[画像:04391.jpg|590px]] | |||
ある水溶液中の水素イオン濃度が真水より高いとき、その溶液は、{~=酸性~アルカリ性}である。 | |||
//LEVEL:2 | //LEVEL:2 | ||
//RAND | //RAND | ||
ある水溶液中の水素イオン濃度が真水より高いとき、その溶液は、{=酸性.~アルカリ性}である。 | ある水溶液中の水素イオン濃度が真水より高いとき、その溶液は、{~=酸性~アルカリ性}である。 | ||
//LEVEL:1 | |||
//RAND | |||
[[画像:04391.jpg|590px]] | |||
ある水溶液中の水素イオン濃度が真水より低いとき、その溶液は、{~酸性~=アルカリ性}である。 | |||
//LEVEL:2 | //LEVEL:2 | ||
//RAND | //RAND | ||
ある水溶液中の水素イオン濃度が真水より低いとき、その溶液は、{~酸性 | ある水溶液中の水素イオン濃度が真水より低いとき、その溶液は、{~酸性~=アルカリ性}である。 | ||
//LEVEL:3 | //LEVEL:3 | ||
//RAND | //RAND | ||
酸の実体とは {~酸素~酸素イオン~水素~=水素イオン}である。 | |||
</GIFT> | </GIFT> | ||
2024年12月18日 (水) 11:30時点における最新版
POINT!
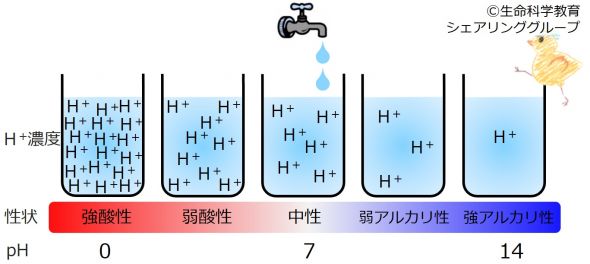
| 水溶液中の水素イオン(H+)が多いほど酸性が強い。逆に、水素イオン(H+)が少ないほどアルカリ性が強い。 |
酸の実体とは、水素イオン(H +)なのです。水溶液中の水素イオン濃度がその溶液の酸性、アルカリ性を決定します。
真水にはH2Oしかないわけではないのです。ある一定濃度の水素イオン(H +)があります。
水素イオン濃度が真水より 低い水溶液は アルカリ性であり、高い水溶液は酸性
です。また、
水素イオン濃度が 低いほどアルカリ性が強く、 高いほど 酸性が強い
のです。
Challenge Quiz
1.

ある水溶液中の水素イオン濃度が真水より高いとき、その溶液は、 酸性 アルカリ性 である。
2.
ある水溶液中の水素イオン濃度が真水より高いとき、その溶液は、 酸性 アルカリ性 である。
3.


ある水溶液中の水素イオン濃度が真水より低いとき、その溶液は、 酸性 アルカリ性 である。
4.
ある水溶液中の水素イオン濃度が真水より低いとき、その溶液は、 酸性 アルカリ性 である。
5.
酸の実体とは 酸素 酸素イオン 水素 水素イオン である。